Cómo usar AlphaFold para modelar proteínas: guía práctica para principiantes
- 9 de diciembre de 2025

Tiempo de lectura: 5 minutos.
La predicción de estructuras proteicas solía ser un proceso caro, lento y reservado para laboratorios con equipos avanzados como cristalografía de rayos X o RMN. Pero desde la llegada de AlphaFold, la inteligencia artificial desarrollada por DeepMind, el campo cambió para siempre.
Hoy, cualquier estudiante, científica o investigador independiente puede predecir la estructura 3D de una proteína desde una laptop… o incluso desde el navegador.
En este blog te explico, paso a paso:
- Qué es AlphaFold
- Cómo funciona
- En qué casos sí (y no) usarlo
- Cómo correr AlphaFold gratis
- Cómo interpretar los resultados
- Aplicaciones reales en ciencia y biotecnología
Tabla de contenidos
¿Qué es AlphaFold?
AlphaFold es un modelo de inteligencia artificial basado en deep learning que predice la estructura tridimensional de proteínas con una precisión comparable a métodos experimentales tradicionales.
Fue creado por DeepMind, y revolucionó la biología estructural al competir en la conferencia CASP —donde superó todos los métodos existentes y logró predicciones con un error de menos de 1 Å en muchos casos.
¿Cómo funciona AlphaFold (simplificado)?
AlphaFold usa:
1. Múltiples secuencias alineadas (MSA)
Busca proteínas similares en bases de datos para aprender patrones evolutivos.
2. Plantillas estructurales
Opcionalmente, usa estructuras conocidas para mejorar la predicción.
3. Redes neuronales profundas
Aprenden relaciones espaciales entre aminoácidos.
4. Un modelo geométrico
Convierte esa información en coordenadas 3D.
El resultado:
Una estructura con valores de confianza llamada pLDDT, que indica qué tan confiable es cada región.
¿Cuándo usar AlphaFold?
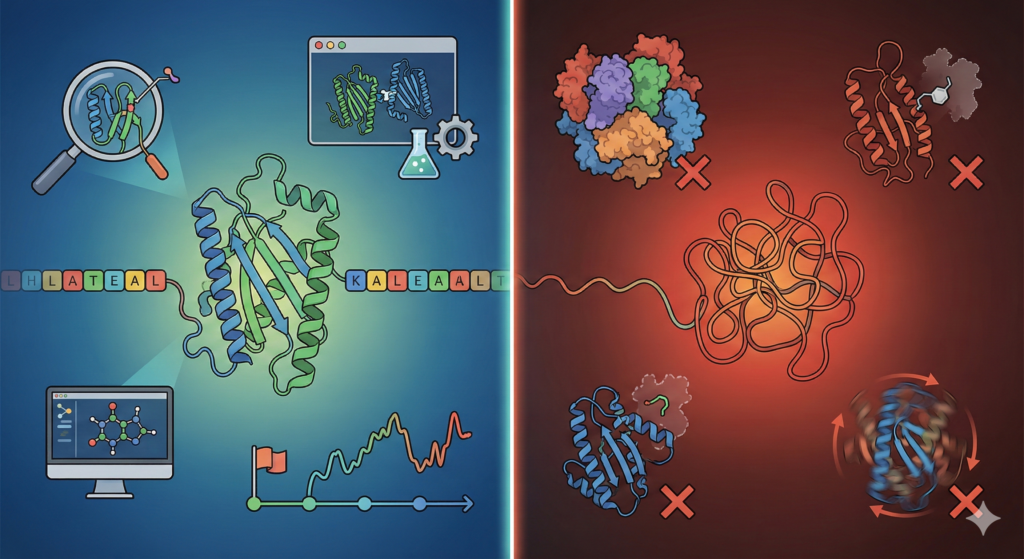
✔ Cuando tienes la secuencia aminoacídica
✔ Para estudiar dominios, plegamientos, mutaciones
✔ Para modelar proteínas pequeñas o medianas
✔ Para biología computacional, docking, diseño racional
✔ Como punto de partida para simulaciones
❌ Cuándo NO usar AlphaFold:
✘ Para proteínas intrínsecamente desordenadas
✘ Para complejos grandes (usa AlphaFold Multimer)
✘ Para estructuras dependientes de ligandos/iones
✘ Para predecir cambios conformacionales dinámicos
Cómo usar AlphaFold GRATIS (paso a paso)
Opción 1: AlphaFold en Google Colab (la más práctica)
No se instala nada. Ideal para estudiantes.
Pasos:
- Entra al notebook público:
→ AlphaFold Colab (DeepMind/Jax) - Pega tu secuencia en formato FASTA
- Elige los parámetros (MSA rápido o completo)
- Da clic en Run
- Descarga los archivos PDB y pLDDT
Ventajas:
- Gratis
- Rápido
- Ideal para usuarios sin experiencia
Desventajas:
- Límites de memoria
No sirve para proteínas muy largas (>1400 aa)
Opción 2: AlphaFold Multimer (para complejos proteicos)
Ideal para dímeros, trímeros o interacciones proteína–proteína.
Notebook recomendado:
→ AlphaFold Multimer Colab
Solo debes pegar cada secuencia en formato FASTA y especificar el número de copias.
Opción 3: Instalar AlphaFold localmente
Solo recomendable si tienes una computadora con:
- GPU NVIDIA ≥ 16 GB RAM
- Linux
- Docker o Conda
Ventajas:
- Resultados rápidos
- Control total
- Puedes correr muchas proteínas
Desventajas:
- Instalación avanzada
- Necesita potencia de cómputo
Cómo interpretar los resultados de AlphaFold
AlphaFold genera tres archivos importantes:
1. Archivo .pdb
Contiene las coordenadas 3D de la proteína.
Puedes visualizarlo en:
- PyMOL
- UCSF ChimeraX
- Mol Viewer (online)*
2. pLDDT (confidence score)
Es un valor entre 0 y 100:
- 90–100: extremadamente confiable
- 70–90: bueno
- 50–70: dudoso
- <50: probablemente desordenado o incorrecto
Usa este valor para interpretar si el modelo es utilizable para docking, mutagénesis, etc.
3. Predicted Aligned Error (PAE)
Indica qué tan precisa es la relación espacial entre dos residuos o dominios.
Muy útil para proteínas modulares o complejos.
Aplicaciones reales de AlphaFold
AlphaFold ya se usa en:
Diseño de fármacos: Modelos iniciales para docking molecular.
Ingeniería de enzimas: Predicción de regiones activas, mutantes, estabilidad.
Biotecnología industrial: Nuevas enzimas para degradar plástico, biosíntesis, biocombustibles.
Ciencia de materiales bioinspirada: Proteínas estructurales, péptidos autoensamblables.
Entender mutaciones en enfermedades: Predicción de efectos estructurales.
Limitaciones que debes conocer
AlphaFold NO predice:
- Estados alternativos
- Cambios conformacionales dinámicos
- Estructuras dependientes de ligandos
- Proteínas con desorden estructural
- Proteínas muy flexibles
- Cinética o dinámica molecular (para eso usa MD)
Aun así, sigue siendo una herramienta revolucionaria.
- Estados alternativos
Conclusiones
AlphaFold democratizó la biología estructural.
Hoy, cualquier científica o estudiante en Latinoamérica puede generar modelos tridimensionales de proteínas en minutos.
Es una herramienta esencial si trabajas en:
- Biología molecular
- Bioquímica
- Biotecnología
- Bioinformática
- Ciencia de materiales
- Química computacional
Y lo mejor: puedes comenzar hoy mismo, gratis.
Recomendación de cursos
Si quieres aprender a usar AlphaFold de manera práctica, te recomiendo el curso:
Recomendación adicional del equipo Conociverso
Diplomado en Bioinformática: formación integral para adquirir competencias avanzadas en análisis computacional y datos biológicos, altamente valoradas en la industria.
Referencias
- Jumper, J. et al. (2021). Highly accurate protein structure prediction with AlphaFold. Nature, 596, 583–589.
- Senior, A. W. et al. (2020). Improved protein structure prediction using potentials from deep learning. Nature, 577, 706–710.
- Varadi, M. et al. (2022). AlphaFold Protein Structure Database: massively expanding the structural coverage of protein-sequence space with high-accuracy models. Nucleic Acids Research, 50(D1), D439–D444.
- DeepMind. AlphaFold: The making of a scientific breakthrough.
https://www.deepmind.com/research/highlighted-research/alphafold - AlphaFold GitHub Repository (DeepMind).
https://github.com/deepmind/alphafold - Mirdita, M. et al. (2022). ColabFold: making protein folding accessible to all. Nature Methods, 19, 679–682.
- Dill, K. A., & MacCallum, J. L. (2012). The protein-folding problem, 50 years on. Science, 338(6110), 1042–1046.
- Baek, M. et al. (2021). Accurate prediction of protein structures and interactions using a three-track neural network. Science, 373(6557), 871–876.
- International Society for Computational Biology (ISCB). AlphaFold Resources.
- Jumper & Hassabis. (2022). Protein structure prediction and the future of structural biology. Annual Review of Biochemistry.

Cuando dos años de trabajo académico desaparecen con un solo clic
El uso de herramientas de inteligencia artificial se ha vuelto cotidiano en la academia, pero no está exento de riesgos. Este artículo analiza un caso reciente publicado en Nature en el que un investigador perdió dos años de trabajo académico tras un cambio en la configuración de privacidad de una plataforma de IA. A partir de esta experiencia, se reflexiona sobre los límites de estas herramientas como espacios de trabajo y la importancia de mantener prácticas sólidas de respaldo y gestión de la información científica.

El café y el microbioma intestinal: evidencia científica de una interacción específica
El café es una de las bebidas más consumidas en el mundo y, durante años, se ha asociado con diversos beneficios para la salud. Pero ¿sabías que también podría influir directamente en las bacterias que viven en tu intestino? Un estudio reciente publicado en Nature Microbiology analizó datos de decenas de miles de personas y encontró que el consumo habitual de café está estrechamente relacionado con la presencia de una bacteria intestinal específica: Lawsonibacter asaccharolyticus. Este hallazgo ofrece una nueva perspectiva sobre cómo lo que bebemos a diario puede modificar nuestro microbioma y, potencialmente, nuestra salud.
Construyendo virus desde cero para combatir superbacterias
La resistencia a los antibióticos es una de las mayores amenazas para la salud global. Frente a este desafío, científicos de New England Biolabs (NEB®) y la Universidad de Yale han desarrollado el primer sistema completamente sintético para diseñar y construir bacteriófagos —virus que infectan bacterias— desde cero. Utilizando información digital de ADN y una innovadora plataforma de ensamblaje genético, esta tecnología permite crear virus altamente específicos capaces de atacar bacterias resistentes como Pseudomonas aeruginosa. Este avance acelera la investigación en fagoterapia y abre la puerta a terapias más seguras, precisas y escalables contra las llamadas “superbacterias”.


