Curso de PCR y Diseño de primers

PhD(c). Luis Mauricio Salazar García
Tecnológico de Monterrey
Curso de PCR y Diseño de primers
Modalidad en video a tu ritmo
Acceso durante 1 año
10 horas totales
$899.00 MXN ($45 USD)
Información general
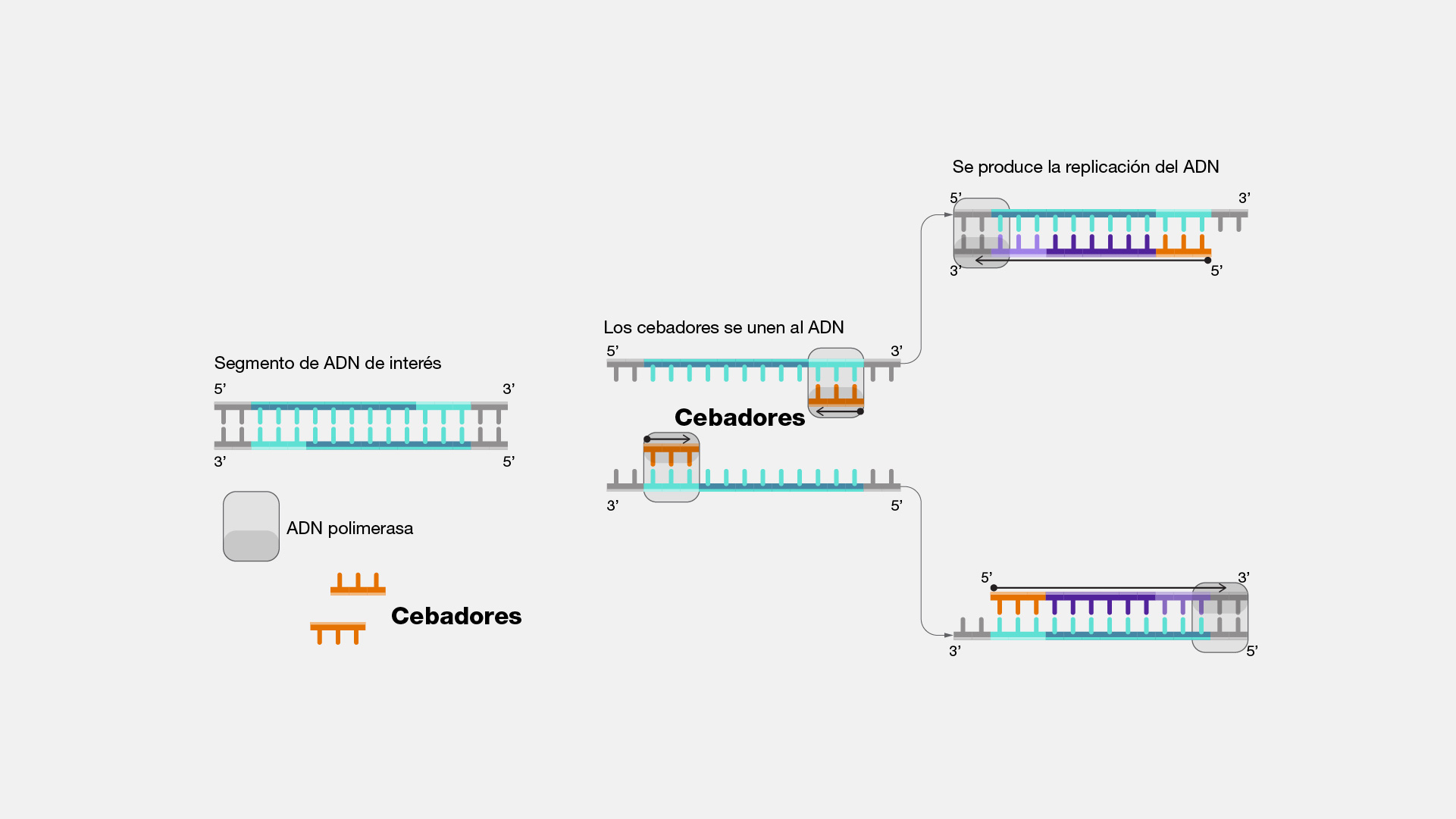
El curso de PCR y Diseño de Primers ofrece una base sólida en biología molecular, enfocándose en la reacción en cadena de la polimerasa (PCR) y el diseño de oligonucleótidos. Los participantes aprenderán a optimizar primers mediante herramientas bioinformáticas y aplicarán estos conocimientos en experimentos como detección y clonación.
Qué aprenderás
A quién va dirigido este curso
El curso de PCR y Diseño de Primers está dirigido a investigadores, estudiantes y profesionales de todos los niveles académicos y laborales que trabajan en el ámbito de la biología molecular. Es ideal para quienes buscan profundizar en el diseño y aplicación de primers en experimentos de PCR, optimizando sus técnicas con herramientas bioinformáticas para mejorar la precisión y eficiencia en sus investigaciones.
Beneficios del curso
Certificado de finalización
Constancia de
finalización del curso
y realización de un
proyecto con valor
curricular
Instructores expertos
Aprende directamente de expertos del área de las mejores instituciones de Latinoamérica y el mundo
Temario
M1 Fundamentos de estructura de nucleótidos y PCR
- Repaso de estructura del DNA. Composición química y enlaces fosfodiéster
- Desoxirribonucleósidos/desoxirribonucleótidos. Ejemplos de modificaciones químicas en nucleótidos y su uso en biología molecular
- Emparejamiento de bases. Proporciones y reglas de Chargaff
- PCR. Concepto básico y etapas, así como herramientas esenciales: plantilla, promers, Taq y dNTPs.
- Elementos de la PCR. Factores clave como laa concentración de MgCl2, ciclo térmico y tamaño del amplicón.
- Variantes de la PCR y su aplicación.
M2 Oligonucleótidos y sus características para amplificación de regiones genéticas.
- Diseño de oligonucleótidos. Criterios de diseño: longitud, Tm, %GC y estabilidad hacia el extremo 3´.
- Software para el diseño. Introducción a herramientas como Primer3, OligoAnalizer y benchling, enfocado al diseño de oligonucleótidos.
- Búsqueda de un gen de interés para realización de un ejercicio. Navegación por las bases de datos para la identificación de las secuencias relevantes.
- Ejercicio práctico 1: Elección de un gen objetivo y diseño de primers específicos para el desarrollo de un sistema de detección. Enfoque para identificación de amplicones de relevancia.
M3 Oligonucleótidos y sus características para la clonación 1/2
- Clonación y expresión de proteínas. Definición de clonación. Características de un plásmido. Vectores como sistemas para la expresión y requerimientos propios.
- Enzimas de restricción. Conceptos y tipos de enzimas. Reconocimiento de sitios de restricción y diseño de oligonicleótidos con sitios compatibles.
- Ejercicio práctico 2. Diseño de oligonucleótidos para la realización de ensamblados moleculares. Desarrollo de la obtención de un gen para la expresión usando herramientas bioinformáticas, enfocado a clonación por enzimas de restricción.
M4 Oligonucleótidos y sus características para la clonación 2/2
- Clonación tipo Golden Gate. Concepto y ventajas como ensamble de múltiples fragmentos. Uso de enzimas tipo IIS.
- Clonación tipo Gibson. Ensamblaje sin enzimas de restricción. Concepto basado en extremos compatibles y como hacer ese diseño de hibridación para los oligonucleótidos.
- Ejercicio práctico 3. Realización de ensamblaje tipo Golden Gate enfocado al diseño de los iniciadores.
- Ejercicio práctico 4. Ensamblado tipo Gibson enfocado a la generación de los extremos compatibles.
M5 Definición de casos prácticos.
- Revisión de casos práctico
- Resolución del primer caso enfocado a la generación de un sistema de detección para un microorganismo patógeno.
- Resolución del segundo caso enfocado a la expresión de la proteína para su posterior estudio.
- Retroalimentación
- Aclaración de dudas generales
Proyecto
Identificación de un fitopatógeno de importancia económica
Se diseñará una metodología para elaborar un sistema de detección basado en PCR. Este caso práctico va dirigido a identificar un hongo que ataca el cultivo de arroz.
Instructor

PhD(c). Luis Mauricio Salazar García
Tecnológico de Monterrey
Es Químico Farmacéutico Biólogo (Q.F.B.) y Maestro en Ciencias (M.C.) con especialidad en Biología Experimental por la Universidad de Guanajuato. Actualmente es candidato a Doctorado en Biotecnología.
Forma parte del equipo de Biología sintética en el Centro de Biotecnología del Tecnológico de Monterrey; enfocado a usar herramientas genéticas novedosas en microorganismos para la producción de moléculas de valor, además de utilizar nuevas cepas como chasis biotecnológico.
Entre sus proyectos principales está la ingeniería genética aplicada a microorganismos no-modelo.
Certificado digital

Obtendrás un certificado con valor curricular, el cual queda registrado dentro de la plataforma de Conociverso y podrás consultar en cualquier momento para su validación.
Requerimientos técnicos
- Se recomienda que el participante tenga conocimientos previos en biología molecular, genética y bioquímica para maximizar el aprovechamiento del curso.
- Memoria RAM de 8 GB o superior.
- Procesadores core i5 similar o superior.
Preguntas frecuentes
¿Se entrega un certificado al finalizar este curso?
Sí. Al terminar el curso recibirás un certificado con valor curricular, emitido por Conociverso, que demuestra las habilidades adquiridas durante el curso.
¿Debo tener algún grado académico específico para inscribirme?
No necesariamente. Recomendamos contar con conocimientos básicos en ciencias biológicas, pero el programa está pensado para adaptarse tanto a estudiantes como a profesionales.
¿Necesito tener instalado algún software antes de iniciar?
No. Durante el diplomado aprenderás a instalar y utilizar cada herramienta paso a paso, con la guía de tus profesores. Únicamente necesitas contar con una computadora con al menos 8 GB de RAM.
Si las clases en vivo ya pasaron, ¿aun así puedo tomar este curso?
¡Por supuesto! Todos nuestros cursos están diseñados para que también los puedas realizar en modalidad asincrónica, a tu propio ritmo y en el horario que mejor se adapte a ti. Tendrás acceso a las grabaciones de todas las clases del curso y al material complementario.
¿Emiten factura fiscal?
Sí, emitimos factura fiscal únicamente para México. Para solicitarla, ve a la configuración de tu cuenta, en la sección de pagos encontrarás la opción de facturación. Debe solicitarse dentro del mismo mes en que se realizó la compra.
Reseñas
Este curso me sirvió mucho para ampliar mi conocimiento en el manejo de software para investigación, igualmente puede aclarar todas mis dudas durante el curso. También me gustó que los docentes nos hayan apoyado y explicado de manera clara todos los temas.

Dr. Alejandro Pech Burgos
Médico
La atención a los estudiantes fue de primera en disposición y amabilidad tanto de los organizadores como de los profesores. Los profesores son personas con mucha experiencia y que siempre se esforzaron en dar lo mejor de sí para que pudiésemos aprender cada tema.

Dra. Patricia Landa
Docente e investigadora, Universidad Autónoma de Chapingo
Recomiendo a Conociverso son súper profesionales y flexibles. Me encanta su servicio al cliente de alta calidad y formalidad. Los cursos son de alta calidad académica y lo mejor de expertos en el área. Y costos asequibles para los principiantes.

Dra. Victoria Edwina Campos García
Docente e investigadora, UNAM
Las clases son muy dinámicas y todos los profesores son expertos en su tema, muchos de ellos son jóvenes investigadores y eso es un plus de motivación que te da el verlos y aprender de ellos.

M.C. José Adrián Coral Góngora
Profesor de cátedra, CINVESTAV UNIDAD MONTERREY
Me gustó mucho que trabajamos con ejemplos reales. Adquiriendo herramientas aplicables a nuestras líneas de investigación. Los instructores siempre atentos, siempre pendientes de responder dudas. Todo el material disponible, y la posibilidad de revisar la grabación del curso muy bueno para los que nos somos expertos.

Dra. Maria Leticia Arena Ortiz
Profesora investigadora, UNAM
M1 Fundamentos de estructura de nucleótidos y PCR
- Repaso de estructura del DNA. Composición química y enlaces fosfodiéster
- Desoxirribonucleósidos/desoxirribonucleótidos. Ejemplos de modificaciones químicas en nucleótidos y su uso en biología molecular
- Emparejamiento de bases. Proporciones y reglas de Chargaff
- PCR. Concepto básico y etapas, así como herramientas esenciales: plantilla, promers, Taq y dNTPs.
- Elementos de la PCR. Factores clave como laa concentración de MgCl2, ciclo térmico y tamaño del amplicón.
- Variantes de la PCR y su aplicación.
M2 Oligonucleótidos y sus características para amplificación de regiones genéticas.
- Diseño de oligonucleótidos. Criterios de diseño: longitud, Tm, %GC y estabilidad hacia el extremo 3´.
- Software para el diseño. Introducción a herramientas como Primer3, OligoAnalizer y benchling, enfocado al diseño de oligonucleótidos.
- Búsqueda de un gen de interés para realización de un ejercicio. Navegación por las bases de datos para la identificación de las secuencias relevantes.
- Ejercicio práctico 1: Elección de un gen objetivo y diseño de primers específicos para el desarrollo de un sistema de detección. Enfoque para identificación de amplicones de relevancia
M3 Oligonucleótidos y sus características para la clonación 1/2
- Clonación y expresión de proteínas. Definición de clonación. Características de un plásmido. Vectores como sistemas para la expresión y requerimientos propios.
- Enzimas de restricción. Conceptos y tipos de enzimas. Reconocimiento de sitios de restricción y diseño de oligonicleótidos con sitios compatibles.
- Ejercicio práctico 2. Diseño de oligonucleótidos para la realización de ensamblados moleculares. Desarrollo de la obtención de un gen para la expresión usando herramientas bioinformáticas, enfocado a clonación por enzimas de restricción.
M4 Oligonucleótidos y sus características para la clonación 2/2
- Clonación tipo Golden Gate. Concepto y ventajas como ensamble de múltiples fragmentos. Uso de enzimas tipo IIS.
- Clonación tipo Gibson. Ensamblaje sin enzimas de restricción. Concepto basado en extremos compatibles y como hacer ese diseño de hibridación para los oligonucleótidos.
- Ejercicio práctico 3. Realización de ensamblaje tipo Golden Gate enfocado al diseño de los iniciadores.
- Ejercicio práctico 4. Ensamblado tipo Gibson enfocado a la generación de los extremos compatibles.
M5 Definición de casos prácticos.
- Revisión de casos práctico
- Resolución del primer caso enfocado a la generación de un sistema de detección para un microorganismo patógeno.
- Resolución del segundo caso enfocado a la expresión de la proteína para su posterior estudio.
- Retroalimentación
- Aclaración de dudas generales

Curso de PCR y Diseño de primers

PhD(c). Luis Mauricio Salazar García
Tecnológico de Monterrey
Modalidad en video
Acceso durante 1 año
10 horas totales
Nivel intermedio
$899.00 MXN ($45 USD)
Accede a todos nuestros cursos
Especialízate y mantente actualizado como científico bajo un precio cómodo
Conociverso Lite
Cancela cuando lo necesites-
Acceso a más de 40 cursos
-
Certificados ilimitados
-
Ruta personalizada de aprendizaje
Conociverso Pro
Acceso completo anual-
Accede a más de 40 cursos
-
Certificados ilimitados
-
Ruta personalizada de aprendizaje
-
Cursos exclusivos
Plan institucional
Planes personalizados para organizaciones-
Cursos o planes personalizados
-
Evaluación y métricas de aprendizaje
-
Descuento dependiendo el tamaño de tu organización


